AstraZeneca AZD7442 - koktajl przeciwciał na COVID-19, ale czy to faktycznie przełom? (komentarz)
Lek AZD7442, wyprodukowany przez firmę AstraZeneca, może być pierwszym realnym sposobem na zminimalizowanie ryzyka wystąpienia ciężkiej postaci COVID-19. Preparat ma co najmniej 50-procentową skuteczność i jest na ostatniej prostej do wprowadzenia na rynek. - W obecnej sytuacji to dużo - mówi nasz ekspert, dr hab. n.med. Tomasz Dzieciątkowski, choć studzi optymizm.
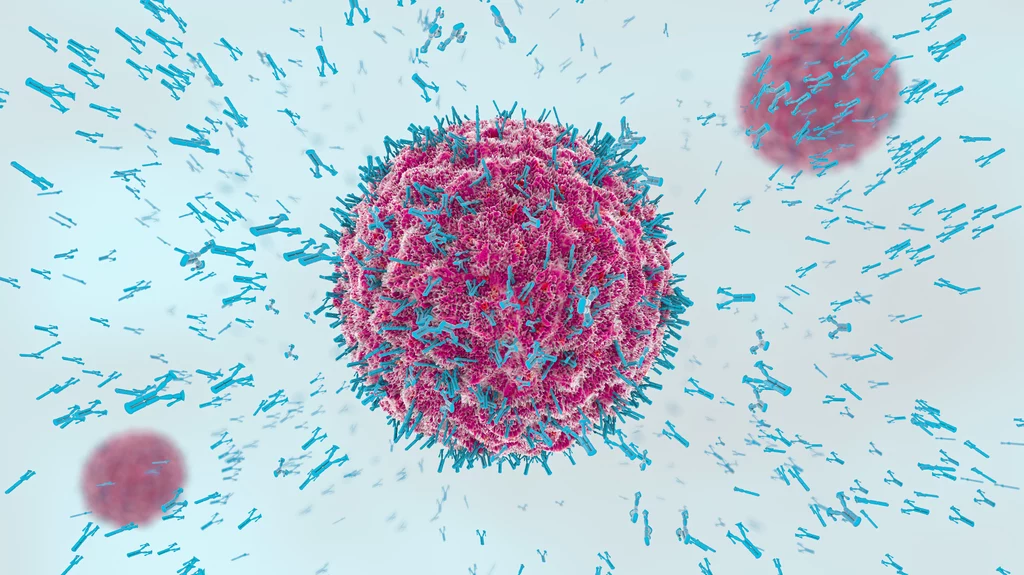
AstraZeneca poinformowała o zakończeniu III fazy badań TACKLE (Tackling Adverse Chemotherapy-associated Late Effects) leczenia COVID-19 przy użyciu AZD7442. Wyniki potwierdzają istotne statystyczne zmniejszenie częstości wystąpienia zgonu i ciężkiej postaci COVID-19. To oznacza, że zastrzyk AZD7442, który jest koktajlem dwóch przeciwciał, jest bezpieczny i stanowi realną ochronę przed ciężką postacią COVID-19.
- Obserwując utrzymujący się na całym świecie wciąż wysoki odsetek poważnych zakażeń wirusem SARS-CoV-2, jako globalna firma farmaceutyczna, czujemy się zobowiązani do poszukiwania nowych rozwiązań profilaktycznych, jak i terapeutycznych, chroniących zdrowie i życie pacjentów przed COVID-19. Naszą szczególną uwagę kierujemy w stronę pacjentów z grup wysokiego ryzyka, osób z zaburzeniami układu odpornościowego, dla których ochrona przeciw COVID-19 jest niezwykle ważna. Wierzymy, że ogłoszone wyniki badań klinicznych dają potencjał zastosowania kombinacji długodziałających przeciwciał w walce z COVID-19 - powiedział nam Piotr Najbuk, Public & Government Affairs Director, AstraZeneca Pharma Poland.AstraZeneca złożyła wniosek do Amerykańskiej Agencji ds. Żywności i Leków (FDA) o zatwierdzenie AZD7442 w celu zapobiegania COVID-19 u osób z grup ryzyka. To może być jeden z najważniejszych momentów naszej walki z pandemią koronawirusa. Zwłaszcza, że niedawno podobny wniosek zgłosiła firma Merck, tyle że w przypadku doustnej pigułki - MK-4482/EIDD-2801 (molnupirawiru).
Ważny krok ku lepszej przyszłości
Wyniki badań potwierdziły, że dawka 600 mg AZD7442 podawana domięśniowo (w formie zastrzyku) zmniejsza ryzyko rozwoju ciężkiej postaci COVID-19 lub zgonu z jakiejkolwiek przyczyny związanej z infekcją SARS-CoV-2 o 50 proc. Grupą kontrolną, która dostała placebo, były osoby z lekką postacią COVID-19, u których objawy choroby występowały przez siedem dni lub krócej. Odnotowano bardzo mało działań niepożądanych - zaledwie 18 w grupie, której podano AZD7442, w porównaniu do 37 incydentów z grupy kontrolnej. To stanowi potwierdzenie, że lek jest bezpieczny i dobrze tolerowany przez organizm.
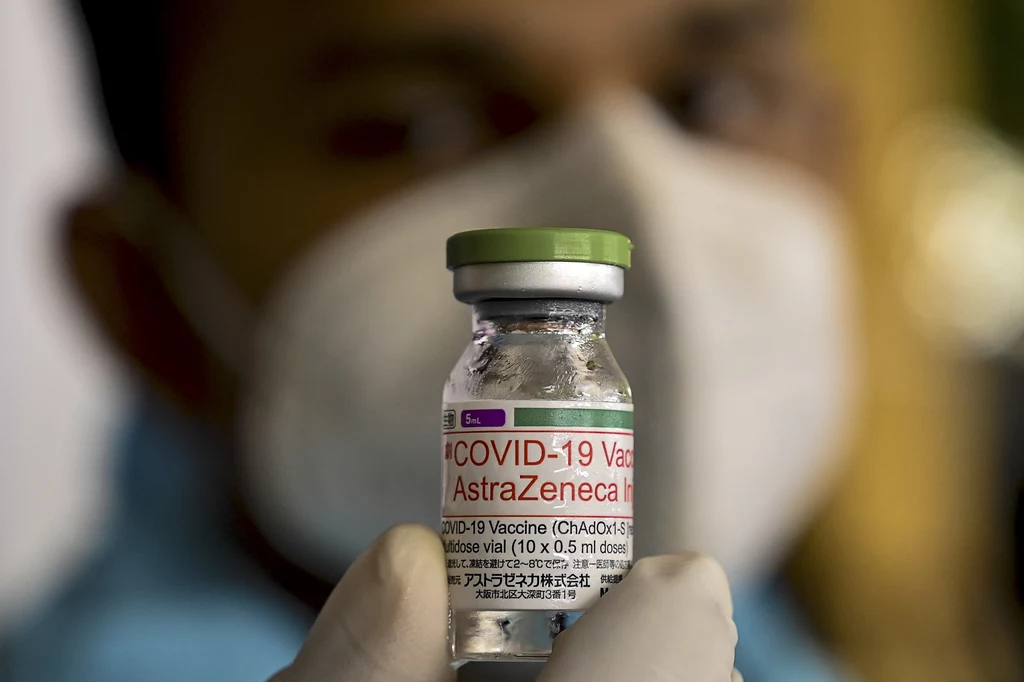
Ważne jest podanie AZD7442 w odpowiednim momencie. Jeżeli preparat zostanie wstrzyknięty w ciągu pięciu dni od wystąpienia objawów COVID-19, zmniejsza ryzyko rozwoju ciężkiej postaci choroby lub zgonu aż o 67 procent (w porównaniu z placebo). Preparat AstraZeneca jest pierwszym, który zarówno chroni przed COVID-19, jak i jest skuteczny w leczeniu samej choroby.- AZD7442, podobnie jak wszystkie inne preparaty oparte na przeciwciałach, przeznaczony będzie wyłącznie do użytku szpitalnego i najprawdopodobniej w pierwszej fazie zakażenia dla pacjentów w stanie średnim, którzy mogą ulec progresji do stanu ciężkiego. To zupełnie inna koncepcja od molnupirawiru, który w założeniach ma być lekiem doustnym, dostępnym powszechnie - powiedział nam dr hab. n.med. Tomasz Dzieciątkowski, wirusolog, mikrobiolog, diagnosta laboratoryjny, doktor habilitowany nauk medycznych, adiunkt w Katedrze i Zakładzie Mikrobiologii Lekarskiej Warszawskiego Uniwersytetu Medycznego oraz asystent w Zakładzie Mikrobiologii Uniwersyteckiego Centrum Klinicznego WUM.
Czym jest AZD7442?
Co takiego niezwykłego jest w AZD7442, że zapewnia tak dużą ochronę przed COVID-19? Jest to połączenie dwóch tzw. długodziałających przeciwciał (LAAB) - tiksagiwimabu (AZD8895) i cilgawimabu (AZD1061) - pochodzących z limfocytów B przekazanych przez pacjentów wyleczonych z COVID-19. Preparat został odkryty przez naukowców z Vanderbilt University Medical Center i jest licencjonowany przez firmę AstraZeneca. Przeciwciała zostały ulepszone - trzykrotnie wydłużono ich okres półtrwania oraz zmniejszono wiązanie receptora Fc i dopełniacza C1q.Badania wykazały, że po podaniu pełnej dawki AZD7442, wysokie stężenie przeciwciał neutralizujących utrzymuje się co najmniej dziewięć miesięcy. W sierpniu 2021 r. AstraZeneca potwierdziła, że AZD7442 zmniejsza ryzyko rozwoju objawowego COVID-19 (badanie PROVENT), a teraz testuje się go jako lek dla hospitalizowanych pacjentów z COVID-19 (badanie ACTIV-3).
Wszystkie przeprowadzone eksperymenty przedkliniczne wykazały, że LAAB-y są w stanie blokować wiązanie wirusa SARS-CoV-2 z komórkami gospodarza, zapewniając tym samym ochronę przed infekcją. Dodatkowo, wiele wskazuje, że AZD7442 działa neutralizująco na warianty Delta i Mu SARS-CoV-2. AZD7442 nie jest jednak lekiem przełomowym, bo nie będzie dostępny dla każdego, a jedynie dla pacjentów hospitalizowanych. Stanowi dobry prognostyk na przyszłość i kierunek, w którym powinny rozwijać się terapie na COVID-19. Mówi o tym jasno nasz ekspert, dr hab. Tomasz Dzieciątkowski.- O ile molnupirawir można uznać za swoisty przełom, to preparatu AZD7442 już tak bym nie określił. Mieliśmy już bowiem do czynienia z lekami biologicznymi opartymi właśnie o przeciwciała monoklonalne. Są one skuteczne, ale tylko w określonym momencie i u określonych pacjentów. Kolejną ich wadą jest wysoka cena. Niemniej pojawia się w ostatnim czasie coraz więcej doniesień na temat nowych preparatów przeciwko SARS-CoV-2. To dobry prognostyk na przyszłość - powiedział nam dr hab. n.med. Tomasz Dzieciątkowski.
Jak przeprowadzono badanie TACKLE?
TACKLE to złożone badania III fazy, randomizowane (uczestnikom zostaje losowo podany lek lub placebo), o podwójnie ślepej próbie (ani pacjent, ani przeprowadzający badanie nie wiedzą, czy podają lek, czy placebo). Badanie przeprowadzono w 96 ośrodkach w Brazylii, Niemczech, Czechach, Węgrzech, Włoszech, Japonii, Meksyku, Hiszpanii, Wielkiej Brytanii, Stanach Zjednoczonych, Rosji, Ukrainie i Polsce. Wzięło w nich udział 903 ochotników - 452. otrzymało AZD7442, a 451. roztwór soli fizjologicznej, w dwóch dawkach domięśniowych.
W badaniu wzięły udział osoby powyżej 18. roku życia, którzy nie byli hospitalizowani i zdiagnozowano u nich łagodną lub umiarkowaną postać COVID-19 (objawy utrzymujące się co najmniej siedem dni). U wszystkich uczestników stwierdzono infekcję SARS-CoV-2 badaniem RT-PCR lub testem antygenowym (wymaz z dróg oddechowych). Około 13 proc. uczestników było po 65. roku życia, a aż 90 proc. miało choroby współistniejące i inne cechy zwiększające ryzyko ciężkiej postaci COVID-19 (np. cukrzycę, astmę, otyłość). Około 62 proc. uczestników badania było rasy białej. AstraZeneca przyjrzała się wpływowi leku w 29. dniu badania TACKLE, a uczestnicy mają być monitorowani przez kolejne 15 miesięcy. Wcześniejsze badania potwierdziły, że koktajl przeciwciał utrzymuje się w organizmie przez co najmniej dziewięć miesięcy od momentu wstrzyknięcia. Długotrwała ochrona (do 12 miesięcy) może być przydatnym dodatkiem dla osób z obniżoną odpornością, których odpowiedź na szczepienie jest niewystarczająca.Wiele wskazuje na to, że AZD7422 zostanie zatwierdzony przez FDA, a wkrótce także inne organy regulacyjne. Proces rejestracji trwa ok. 6-10 tygodni, a po tym czasie można spodziewać się pozwolenia i wprowadzenia leku do szpitali.










