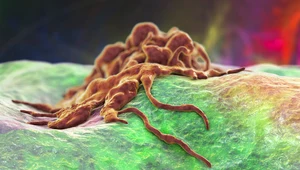
Brazylijczycy opracowali nowy sposób walki z czerniakiem
Brazylijscy naukowcy opracowali peptyd o nazwie Rb4, który jest skuteczny w zwalczaniu czerniaka. Cząsteczka ta może stać się podstawą przyszłych terapii przeciwnowotworowych.
Badania przedkliniczne in vitro i in vivo wykazały, że Rb4 wywołuje martwicę w komórkach czerniaka myszy i hamuje żywotność ludzkich komórek nowotworowych. Badane komórki nowotworowe traciły integralność swoich błon plazmatycznych, a mitochondria (organelle wytwarzające energię) rozszerzały się nawet przy braku kondensacji chromatyny - morfologicznego znaku rozpoznawczego apoptozy. Naukowcy przyznają, że sposób, w jaki dochodzi do tej martwicy, jest wciąż słabo poznany.
U myszy peptyd zmniejszył przerzuty do płuc i spowolnił wzrost podskórnego czerniaka. Wyniki sugerują, że Rb4 działa bezpośrednio na guzy, indukując ekspresję dwóch wzorców alarmin - struktur molekularnych związanych z uszkodzeniem i zagrożeniem (DAMP), które wywołują immunogenną śmierć komórek czerniaka.
- Zajmujemy się naukami podstawowymi, poszukując nowych cząsteczek. W badaniu Rb4, który pochodzi od białka proteolipidowego 2 (PLP2), wykazywał preferencje do wywoływania martwicy, specyficznego rodzaju śmierci komórek, zwłaszcza w czerniaku, ale nie jest jasne, jak ta martwica powstaje i jak się rozwija. W artykule omówiono niektóre aspekty składu morfologicznego peptydu oraz końcowe efekty kontaktu z nim - powiedział Fabrício Castro Machado, współautor artykułu.
Jak działa Rb9?
W 2016 r. naukowcy opisali strukturę Rb9 i jego mechanizm działania jako inhibitora komórek czerniaka. W artykule opublikowanym w 2020 r. wykazano, że Rb9 działa jako immunomodulator i może być wykorzystywany do kontroli progresji nowotworu.
Nowe metody leczenia nowotworów opracowane w ostatnich latach obejmują chemioterapię opartą na peptydach - cieszą się one rosnącym zainteresowaniem nie tylko dlatego, że mogą wiązać się z błonami komórek nowotworowych, ale także dlatego, że mają niską masę cząsteczkową, dobrze przenikają do tkanek komórkowych i są mało toksyczne dla tkanek prawidłowych. Mogą być stosowane jako odczynniki komórkowe, ligandy, szczepionki i nośniki leków cytotoksycznych w terapii samodzielnymi peptydami lub materiałami sprzężonymi z peptydami.
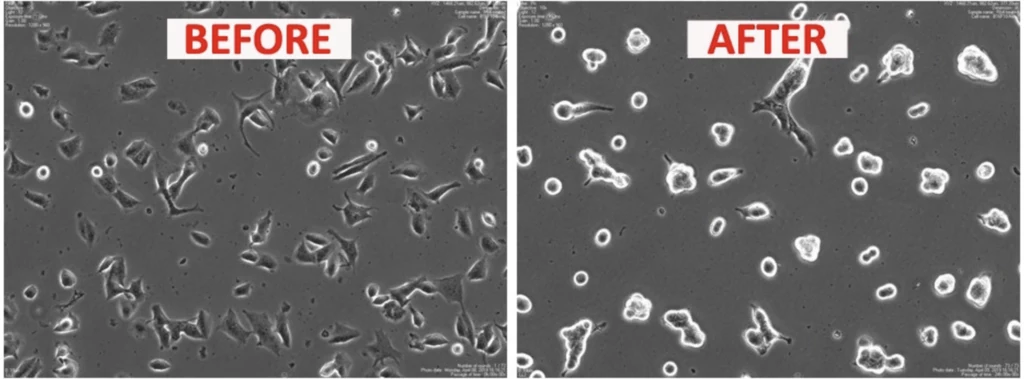
W badaniach nad działaniem przeciwnowotworowym Rb4 grupa naukowców stwierdziła, że peptyd zaburza morfologię, replikację i łączenie się hodowanych w laboratorium komórek czerniaka B16F10-Nex2. W przeciwieństwie do komórek kontrolnych, komórki poddane działaniu Rb4 nie replikowały się i tworzyły skupiska, tracąc swoją naturalną morfologię po inkubacji trwającej co najwyżej 24 godziny.
Ponadto, Rb4 zmniejszył liczbę guzków przerzutowych w płucach w syngenicznym modelu czerniaka (obejmującym tkanki nowotworowe pochodzące od myszy o tym samym składzie genetycznym). Wynik ten został wykryty po wstrzyknięciu komórek czerniaka dożylnie myszom. Myszy otrzymały pięć dootrzewnowych wstrzyknięć peptydu (300 mg na zwierzę) w kolejnych dniach, co opóźniło wzrost guza nawet o 40 dni. Przeżywalność myszy, którym podawano Rb4, była znacznie większa niż myszy z grupy kontrolnej, zwiększając przeżywalność grupy o ponad 25 proc. i do 10 dni.
Czerniak powstaje w komórkach produkujących melaninę, pigment nadający kolor skórze. Może pojawić się w różnych częściach ciała. Chociaż rak skóry jest najczęstszą postacią raka w Brazylii, stanowiąc około 30 proc. wszystkich przypadków, czerniak stanowi jedynie 3 proc. nowotworów złośliwych. Stanowi on jednak największe zagrożenie życia ze względu na wysokie prawdopodobieństwo rozprzestrzenienia się na inne narządy.